Биогеохимический цикл фосфора¶
Химический элемент¶
Фосфор является распространённым химическим элементом, его кларк в литосфере составляет 0,1 %, а в биосфере — 0,05 %.
Фосфор — минералогический элемент, для него известно 239 минералов, самым распространённым из которых является апатит, который содержит 95 % всего фосфора в земной коре и его разновидности. Суммарная масса элемента в гранитном слое литосферы равна 6,33 × 1015 т. В толще осадочных пород сосредоточено 1,311 × 1015 т элемента. Суммарное количество фосфора в осадочной оболочке и гранитном слое континентального блока земной коры равно 7,08 × 1015 т. Следовательно, за 600–700 млн лет было вынесено более 17 % всей массы фосфора, находившегося в гранитном слое литосферы.
Фосфор — жизненной важный элемент. Среднее содержание фосфора в почвах — 0,08 %. Нормальным для интенсивного земледелия в развитых странах считается содержание подвижного P2O5 ~ 300 мг на 1 кг почвы. Для территории СНГ средневзвешенное содержание составляет всего ~ 78 мг/кг при ещё более низких для ряда областей России (Центральное Нечерноземье, Север, Сибирь и так далее).
Фосфор — главный биофильный (коэффициент концентрации в живом веществе относительно литосферы) и биогенный (элемент, постоянно входящий в состав организмов и имеющий конкретное биологическое значение) элемент.

Фосфор абсолютно необходим всем организмам, поскольку входит в состав нуклеиновых кислот, некоторых липидов, а также ряда веществ, служащих аккумуляторами и передатчиками энергии, таких как АТФ (аденозин-трифосфорная кислота), АДФ (аденозин-дифосфорная кислота) и НАДФ (никотин-амида-денин-динуклеотид-фосфат). Фотосинтез, дыхание, брожение, синтез белка — все эти процессы происходят при участии фосфорсодержащих веществ. Для позвоночных животных фосфор важен также как компонент костной ткани.
Относительное содержание фосфора в организмах невелико. По числу атомов фосфора нужно в 15 раз меньше, чем азота, и в 100 раз меньше, чем углерода. Однако на огромных просторах океана, а также в озёрах и водохранилищах нехватка именно этого биогенного элемента часто оказывается основным фактором, ограничивающим развитие фитопланктона, а следовательно, и всех последующих звеньев трофической цепи. В наземных экосистемах первичная продукция лимитирована фосфором реже, однако получать устойчивые высокие урожаи сельскохозяйственных культур без регулярного применения фосфорных удобрений невозможно.
Среднее содержание фосфора в сухой массе живых организмов наземных экосистем составляет около 0,2 %, в океанических — около 1,1 %. Значительная часть запасов этого элемента сосредоточена в почвенном гумусе, в котором содержание фосфора в среднем равно 0,15 % и который служит биогеохимическим барьером в наземном цикле этого элемента. Общая масса фосфора в биотической и абиотической материи составляет около 9,7 × 109 т (до 200 Гт).
В живом веществе суши до воздействия человека находилось около 5 × 109 т фосфора, в биомассе фотосинтетиков океана его содержится 0,03–0,04 × 109 т. Значительная часть элемента сохраняется в почвенном органическом веществе педосферы, в котором концентрация фосфора около 0,15 %, а масса соответственно около 7 × 109 т. Достоверно оценить массу фосфора, находящегося в минеральной части почв, пока невозможно.
Цикл фосфора¶
Среди набора обязательных для всех организмов элементов (C, H, N, O, P и S) биогеохимический цикл фосфора сильно отличается от биогеохимических циклов углерода, кислорода, азота и серы, так как газовая форма соединений фосфора (например, PH3) практически не участвует в биогеохимическом цикле фосфора. По воздуху он может переноситься только с пылью или в виде солей, образовавшихся при высыхании морских брызг. Основные перемещения фосфора по поверхности Земли происходят вместе с водой. Это так называемый осадочный цикл, в ходе которого фосфор, находящийся в горных породах, при химическом их выветривании под действием слабых кислот переводится в растворимые формы и сносится речными водами в океан, где постепенно накапливается в донных отложениях. Возврат на сушу происходит только при подъеме дна в результате тектонических процессов, а также при снижении уровня океана во время оледенений. Организмы встраиваются в это движение фосфора по поверхности планеты, приспосабливаются к экономному использованию этого дефицитного элемента, иногда образуют небольшие локальные петли повторной его утилизации (рециклинга), но не определяют течение всего цикла в глобальных масштабах.
В некоторых местах возврат фосфора из моря на сушу происходит за счёт деятельности организмов. Речь идёт о птичьих базарах — колониях птиц, гнездящихся на берегу (преимущественно на островах, где нет наземных хищников), но добывающих себе пищу (главным образом мелкую рыбу) в море. Залежи гуано (помета этих птиц) — ценнейшее удобрение, содержащее азот и фосфор в форме, пригодной для использования растениями. Однако в целом, в масштабах всей биосферы, вклад подобной биогенной составляющей в перемещение фосфора крайне мал.
В отложениях на дне океана содержатся основные запасы фосфора — около 4–10 Гт. В водной толще фосфора сравнительно немного — около 90 Гт, причём почти весь он сосредоточен в глубинных водах в виде \(\ce{PO4^3-^}\), \(\ce{PO4^2-^}\) и других анионов, а также в составе органических соединений. В поверхностных слоях этот элемент, находящийся в форме доступной для использования планктоном, сразу же им и потребляется, а затем передаётся дальше по цепям питания. Возврат его во внешнюю среду происходит при отмирании организмов, а также с продуктами выделения планктонных ракообразных и других животных в ходе их обычного метаболизма. На суше довольно много фосфора находится в почвах — в сумме около 200 Гт. Запасы фосфора в апатите и других горных породах, которые в настоящее время рентабельно использовать в качестве источника минеральных удобрений, сравнительно невелики — около 10 Гт. К этим запасам, безусловно, следует относиться очень бережно, так как в масштабах времени существования человеческой цивилизации они фактически являются невозобновляемыми ресурсами.
При выветривании фосфорсодержащих пород высвобождаются ионы фосфата \(\ce{PO4^2-^}\), которые в кислой среде связываются с железом или алюминием, а в щелочной — с кальцием. Соответственно, в почве фосфор наиболее доступен для использования растениями при значениях pH около 6–7. Попадая в пресные воды, ионы фосфата интенсивно поглощаются фитопланктоном, но, кроме того, существует и чисто химический механизм связывания фосфора с железом. В море этот механизм менее эффективен, поскольку там железо взаимодействует прежде всего с имеющимися в большом количестве ионами сульфата. При выпадении над континентами кислых дождей в озера попадает серная кислота, что также ведёт к высвобождению дополнительного количества фосфора и повышению первичной продукции водоёмов.
Для подавляющего большинства пресноводных экосистем фосфор является основным фактором, лимитирующим первичную продукцию. Сама зависимость уровня развития фитопланктона от поступления в водоём фосфора стала очевидна в 60–70-х годах 20 века, когда в развитых странах Европы и Северной Америки стали в большом количестве применять минеральные удобрения и фосфорсодержащие моющие средства — детергенты. Именно тогда широко распространилось явление антропогенного эвтрофирования — превращения озёр олиготрофных («малопитательных», характеризующихся низкой первичной продукцией и поэтому чистой прозрачной водой) и мезотрофных (со средней величиной первичной продукции) в эвтрофные («высокопитательные») и даже «гиперэвтрофные» (получающие ненормально большое количество элементов минерального питания для водорослей и цианобактерий).
Для эвтрофных водоёмов характерно явление необычайно бурного развития фитопланктона, называемое «цветением воды». Вода при этом становится зелёного цвета (иногда — с бурым или синеватым оттенком) и малопрозрачной. Многие вызывающие «цветение» водоросли и цианобактерии образуют крупные колонии и тем самым становятся крайне неудобными для поедания их ракообразными-фильтраторами. Кроме того, некоторые цианобактерии ядовиты для планктонных животных. В результате потребление фитопланктона зоопланктоном существенно снижается. Даже в тех случаях, когда в фитопланктоне доминируют мелкие съедобные водоросли, рост их численности и биомассы может быть столь быстрым, что планктонные животные не могут его сдержать. Не потреблённая планктонными животными масса фитопланктона начинает отмирать и опускается на дно, давая пищу огромному количеству гетеротрофных бактерий, которые, перерабатывая это вещество, нередко поглощают практически весь кислород в придонной зоне. В возникших анаэробных условиях деструкция органического вещества протекает значительно медленнее, а на дне начинают интенсивно накапливаться иловые отложения. Усилению процесса эвтрофирования способствует и то, что в отсутствие кислорода из соединений фосфора, находящихся в донных отложениях, начинают высвобождаться ионы фосфата (вследствие замещения фосфора железом) и, соответственно, фитопланктон получает дополнительную подпитку.
Эвтрофные, а тем более гиперэвтрофные водоёмы нельзя использовать для водоснабжения. В них исчезают многие ценные промысловые виды рыб (например, лососёвые), поскольку они обычно чувствительны к снижению концентрации кислорода, а недостаток его в эвтрофных водоёмах наблюдается очень часто, причём не только в придонных слоях водной толщи, но иногда и близко к поверхности (например, ночью, когда фотосинтез не идёт, а дыхание фитопланктона продолжается и на него расходуется очень много кислорода).
Борьба с эвтрофированием, ставшая особенно актуальной в 70-х годах XX века, оказалась необычайно трудной и дорогостоящей. Ведь фосфат сам по себе не считается загрязнителем. Более того, он абсолютно необходимый компонент минеральных удобрений, которые повсюду применяются на полях и поэтому в большем или меньшем количестве всегда попадают в ручьи и реки, а из них в озера и водохранилища.
Однако установить связь между поступлением в водоём фосфора извне и количеством развивающегося фитопланктона не так просто. Дело в том, что этот крайне дефицитный элемент сейчас же потребляется водорослями и бактериями, а в воде концентрация его в доступной форме оказывается очень низкой, нередко на пределе возможностей аналитических методов.
Поэтому для водоёмов средней полосы России летом, в период бурного развития фитопланктона, значимой корреляции между его количеством и содержанием растворенного фосфора (везде очень низким) может и не выявиться. Но если для большой группы водоёмов концентрацию фосфора в воде измерить весной, сразу после того, как сойдёт снег, и пока ещё не началось массовое развитие водорослей, а биомассу фитопланктона — летом, когда она близка к максимальной, то, скорее всего, между этими величинами будет обнаружена чёткая положительная корреляция. Такие измерения не раз проводились. Смысл зависимости понятен: количество развивающегося фитопланктона пропорционально тому количеству фосфора, которое поступило в водоём с территории водосбора.
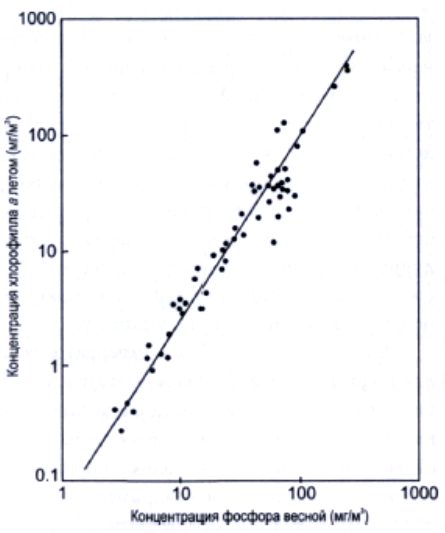
Поскольку фосфор, по-видимому, всегда был очень дефицитным элементом, у бактерий и водорослей уже на ранних этапах эволюции должна была сформироваться способность к потреблению его при крайне низком содержании в среде. Согласно, например, обследованию 56 озёр умеренных широт Северной Америки показано, что концентрация фосфата в них колебалась от 30 до 900 пикомолей (10–12 моль/л), со средним значением 174 пикомоля. Это на два и даже на три порядка меньше, чем предполагалось ранее, при использовании менее совершенной методики оценки. При потреблении элементов в столь низких концентрациях в более выигрышном положении оказываются самые мелкие формы, так как у них выше отношение поверхности к объёму.
Рециклинг фосфора в планктонном сообществе. Зоопланктон получает необходимый ему фосфор из пищи — планктонных водорослей, цианобактерий, частиц детрита (и поселившихся на них гетеротрофных бактерий). В процессе своей жизнедеятельности планктонные животные выделяют фосфор во внешнюю среду, причём по крайней мере половина его поступает в форме, доступной для немедленного использования фитопланктоном. Кроме того, фосфор возвращается в круговорот при разложении отмирающих клеток водорослей и бактерий. Практически всегда сохраняющаяся острая потребность фитопланктона в минеральном фосфоре приводит к тому, что как только он поступает в среду, то сразу же снова потребляется цианобактериями и водорослями. Расчётное время рециклинга фосфора в планктонном сообществе составляет от нескольких минут (при низкой концентрации его в среде) до получаса и даже часа (при более высокой концентрации).
Отсюда очевидно, что для правильной оценки роли фосфора в ограничении продукции фитопланктона важно знать не только содержание этого элемента в среде, но и скорость его обращения. Это справедливо по отношению к любому химическому элементу, потребляемому живыми организмами, но в случае фосфора в водной среде проявляется особенно наглядно. Когда летом в озере устанавливается температурная стратификация (а это значит, что водная толща не перемешивается и приток биогенных элементов из придонных слоёв невозможен), то практически вся первичная продукция в верхних слоях поддерживается почти исключительно за счёт фосфора, поступающего с продуктами экскреции зоопланктона. При этом чем интенсивнее питаются планктонные животные, тем интенсивнее происходит выделение ими фосфора. Скорость экскреции меняется в зависимости от температуры, а также от массы тела планктонных животных, примерно так же, как скорость дыхания. В расчёте на единицу массы у более мелких форм она существенно выше, чем у крупных.
Фосфор в океане. Соотношение фосфора и азота. В океан фосфор попадает со стоком рек как в растворенном состоянии, так и во взвешенном. Благодаря высокому содержанию углекислого газа и гуминовых кислот речные воды имеют слабокислую реакцию, что способствует образованию в них комплексных соединений фосфора с железом. Однако когда эти воды смешиваются с океаническими (обычно характеризующимися слабощелочной реакцией), то часть связанного фосфора высвобождается и становится доступной фитопланктону, способствуя тем самым поддержанию высокой первичной продукции эстуарных экосистем.
В верхних слоях водной толщи растворенный минеральный фосфор (главным образом в виде ионов PO4) сразу же потребляется цианобактериями и водорослями. Океанологи давно ведут спор о том, какой элемент минерального питания, азот или фосфор, чаще всего лимитирует развитие морского фитопланктона. Дело в том, что результаты огромного числа измерений содержания азота и фосфора (в форме, пригодной для использования фитопланктоном) по всей акватории Мирового океана показывают, что между ними существует очень чёткая положительная корреляция. Нет таких мест в океане, где было бы много азота, но мало фосфора, и, наоборот, таких, где было бы мало азота, но много фосфора.
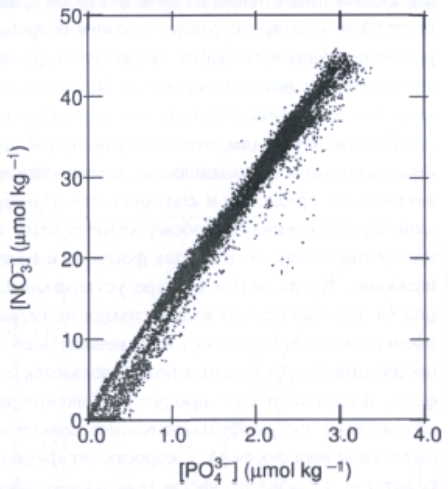
Столь тесная связь между концентрациями в среде этих двух важнейших биогенных элементов является результатом жизнедеятельности организмов, потребляющих и выделяющих азот и фосфор в строго определённых соотношениях.
Надо также учитывать и то, что элементы эти попадают в океан разными путями: азот — с речным стоком, а также за счёт азотфиксации из атмосферы; фосфор — только с речным стоком. Соответственно, в случае нехватки в поверхностных водах океана азота она может быть восполнена деятельностью азотфиксаторов (поглощающих нужный им азот из практически неограниченного запаса его в воздухе), но если не хватает фосфора, то его взять неоткуда. А из этого следует, что по крайней мере в масштабах геологического времени определяющая роль в ограничении первичной продукции принадлежит фосфору, а не азоту. Азотфиксация только «подстраивается» под изменения в притоке фосфора, зависящие от тектонических процессов и циклов оледенений (и связанных с ними изменений в уровне океана).
При этом невольно возникает вопрос, почему же тогда азот, а не фосфор часто рассматривается в качестве основного фактора, лимитирующего первичную продукцию. Основанием для этого служит усреднённое по большому числу данных соотношение азота и фосфора в поверхностных слоях водной толщи океана. Оно оказывается равным 14,7:1, а не 16:1, как следует из соотношения Редфильда (в составе морского фитопланктона соотношение числа атомов углерода, азота и фосфора (C:N:P) составляет в среднем 106:16:1. Т. е. на один атом фосфора планктонным водорослям и цианобактериям требуется шестнадцать атомов азота и сто шесть атомов углерода. Эта пропорция называется соотношением Редфильда). Такой результат может быть следствием недостатка железа, которого азотфиксаторам требуется довольно много. Кроме того, следует учитывать, что в некоторых местах довольно интенсивно протекает деятельность бактерий-денитрификаторов, ведущая к обеднению вод азотом, находящимся в доступной для фитопланктона форме.
В любом случае важно то, что атмосферный азот, связанный азотфиксаторами для собственных нужд (что потребовало от них немалых энергетических затрат), достаётся в конце концов всему сообществу организмов, населяющих океан. Ведь когда азотфиксаторы отмирают и их вещество подвергается бактериальной деструкции, то азот и фосфор поступают в окружающую среду в тех соотношениях, в которых они присутствовали в составе живых организмов. Кроме того, многие цианобактерии потребляются животными, а в веществе их тел отношение N:P гораздо строже поддерживается как 16:1. Соответственно, в таком же соотношении поступают от них азот и фосфор при отмирании. Иначе говоря, получается, что все сообщество пелагических (в толще воды кроме придонной части) организмов как бы направленно работает на поддержание в воде концентраций N и Р в пропорциях, близких к тем, что задаются соотношением Редфильда.